Interrompere il dialogo tra cellule tumorali e linfonodi per battere la leucemia linfatica cronica
Ultimo aggiornamento: 25 gennaio 2021
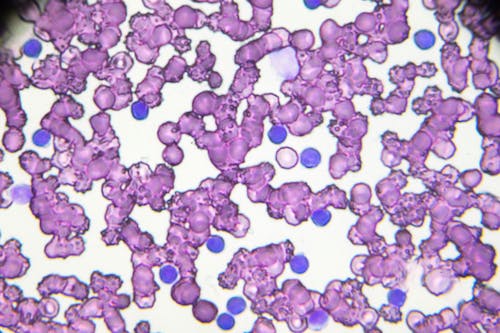
Titolo originale dell'articolo: Enhanced IL-9 secretion by p66Shc-deficient CLL cells modulates the chemokine landscape of the stromal microenvironment
Titolo della rivista: Blood
Data di pubblicazione originale: 12 novembre 2020
Un’anomalia nella produzione della proteina p66Shc è alla base dei processi che portano i linfociti leucemici ad accumularsi nei linfonodi, dove sono protetti dall’attacco del sistema immunitario e dei trattamenti farmacologici.
“La cellula tumorale è come una preda che cerca una tana per evitare di essere aggredita dal sistema immunitario o dai farmaci. Un rifugio ideale è l’ambiente stromale dei linfonodi, che la cellula tumorale è anche in grado di rendere più accogliente, una volta penetrata là dentro.”
Con questa metafora Cosima Baldari, professoressa all’Università di Siena, spiega i risultati di uno studio di cui è coordinatrice, che descrivono il meccanismo attraverso cui, nella leucemia linfatica cronica, le cellule tumorali si accumulano nei linfonodi eludendo i trattamenti farmacologici e alimentando la malattia.
La leucemia linfatica cronica è caratterizzata da una produzione abnorme di linfociti B anomali. “Esattamente come i linfociti sani, anche quelli tumorali passano in continuazione dal sangue alla linfa e viceversa, fermandosi nei linfonodi, dove ricevono segnali per proliferare e rimanere in vita” spiega Baldari, la cui attività di ricerca è sostenuta anche da Fondazione AIRC.
Le cellule tumorali, però, cercano di sfruttare questo processo a proprio favore e di colonizzare i linfonodi, che rappresentano un ambiente favorevole per sopravvivere e moltiplicarsi.
Qualche tempo fa, il gruppo di ricerca coordinato da Baldari aveva scoperto il meccanismo che attrae le cellule leucemiche verso i linfonodi: fisiologicamente queste piccole ghiandole disseminate in tutto il corpo richiamano i linfociti rilasciando segnali chimici (chemochine). I linfociti tumorali sono particolarmente efficaci nel captare questi segnali perché possiedono più recettori per le chemochine rispetto alle cellule sane. Questa caratteristica è la conseguenza di un’anomalia funzionale delle cellule tumorali: la scarsa espressione di un gene chiamato p66Shc.
“In questo nuovo studio, condotto in collaborazione con il gruppo del professor Giampietro Semenzato dell’Università di Padova, abbiamo voluto guardare il fenomeno dalla parte dei linfonodi. Abbiamo così scoperto che c’è un dialogo continuo tra le cellule stromali e le cellule tumorali. La carenza di p66Shc, infatti, ha un’altra conseguenza sulle cellule leucemiche: le induce a rilasciare interleuchina 9, la quale a sua volta causa un maggiore rilascio di chemochine da parte delle cellule stromali. In tal modo si innesca un circolo che si autoalimenta e che ha come effetto di richiamare nei linfonodi sempre più cellule tumorali e di favorirne la permanenza” dice ancora la ricercatrice.
La scoperta di questo meccanismo di base fa ora immaginare nuove potenziali strategie per limitare l'accumulo di cellule tumorali nei linfonodi e “stanare” quelle che vi si sono già insediate, rendendole vulnerabili all’attacco del sistema immunitario o di trattamenti farmacologici. “In esperimenti con animali di laboratorio abbiamo osservato che usando farmaci che neutralizzano l’interleuchina 9 si ha un migliore decorso della malattia, dal momento che viene ridotta la produzione di chemochine e di conseguenza le cellule tumorali non riescono ad accumularsi nei linfonodi. Un’altra possibilità è intervenire ancora più a monte del processo, ripristinando l’espressione di p66Shc. Anche questo approccio si è dimostrato efficace negli animali di laboratorio. L’applicazione negli esseri umani, però, richiede ancora molto lavoro” conclude Baldari.
Antonino Michienzi