Tumore della mammella: ecco come “fluidifica” e diventa invasivo
Ultimo aggiornamento: 30 luglio 2019
Titolo originale dell'articolo: Unjamming overcomes kinetic and proliferation arrest in terminally differentiated cells and promotes collective motility of carcinoma
Titolo della rivista: Nature Materials
Data di pubblicazione originale: 22 luglio 2019
Individuato un meccanismo molecolare che rende “fluido” il carcinoma duttale mammario, promuovendone la metastatizzazione. La scoperta potrebbe portare a trattamenti sempre più mirati e allo sviluppo di nuove terapie.
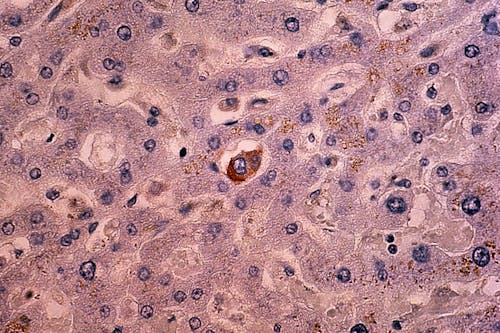
Il carcinoma duttale è una forma frequente di carcinoma della mammella. Si sviluppa nel dotto ghiandolare mammario, dove in genere rimane confinato e immobile come una massa solida. Si parla di carcinoma duttale in situ per via della compressione e limitazione esercitata dal tessuto che lo circonda. Eppure, circa il 30 per cento dei carcinomi duttali della mammella può sviluppare una speciale fluidità che rende più semplice l'invasione del tessuto circostante da parte del tumore e la formazione di metastasi. A chiarire i meccanismi molecolari alla base di questa trasformazione sono ora i risultati pubblicati sulla rivista Nature Materials di uno studio condotto dal gruppo di ricerca di Giorgio Scita presso l'IFOM di Milano, in collaborazione con quello di Roberto Cerbino, professore di fisica applicata all'Università di Milano. Lo studio è stato possibile grazie all'essenziale contributo di AIRC.
Tutto ruota intorno alla proteina RAB5A, di cui già un paio d'anni fa le équipe di Scita e Cerbino avevano chiarito alcune funzioni, come quelle di regolare la capacità delle cellule di portare al proprio interno recettori di membrana e modulare l'adesione reciproca tra cellule. “Inoltre avevamo osservato che RAB5A può indurre la fluidificazione di un tessuto epiteliale denso e compatto” afferma Scita. Ma era anche noto che RAB5A è presente a livelli più alti del normale nei tumori più aggressivi della mammella: da qui l'idea di verificarne il ruolo nella loro progressione.
Per la nuova ricerca Scita e colleghi hanno lavorato sia con speciali modelli cellulari tridimensionali (sferoidi costituiti da cellule tumorali con elevati livelli di RAB5A) sia con animali di laboratorio (topolini). “Abbiamo analizzato la dinamica del movimento delle cellule con l'aiuto di nuovi algoritmi matematici messi a punto dal gruppo di Cerbino” spiega Scita. “Abbiamo osservato che, in presenza di elevati livelli di RAB5A, le cellule tumorali iniziano a ruotare in modo prolungato e che questo movimento deforma la matrice extracellulare, generando delle vie di fuga che permettono alle cellule stesse di invadere il tessuto circostante.” In più i ricercatori hanno chiarito i passaggi molecolari alla base di questi effetti, raccogliendo informazioni che potrebbero rivelarsi utili nella pratica clinica.
“L'obiettivo a breve termine” conclude Scita “è utilizzare le alterazioni strutturali in senso fluidificante indotte alle cellule da RAB5A come marcatori per predire l'evoluzione del carcinoma duttale in situ. Così potremmo identificare in modo più mirato le donne a maggior rischio di progressione, evitando o limitando il trattamento per le pazienti a minor rischio. A lungo termine l'obiettivo è caratterizzare nel dettaglio le vie biochimiche dipendenti da RAB5A verso le quali indirizzare nuove terapie, per bloccare sul nascere il processo di disseminazione tumorale.”
Valentina Murelli